В новом исследовании в клетках исследователи из Университета штата Иллинойс адаптировали технологию редактирования генов CRISPR, чтобы заставить внутреннее оборудование клетки пропускать небольшую часть гена при переписывании его в шаблон для создания белка. Это дает исследователям способ не только устранить мутированную последовательность генов, но и влиять на то, как ген экспрессируется и регулируется.
Такое целевое редактирование могло бы в один прекрасный день быть полезным для лечения генетических заболеваний, вызванных мутациями в геноме, таких как мышечная дистрофия Дюшенна, болезнь Хантингтона или некоторые виды рака.
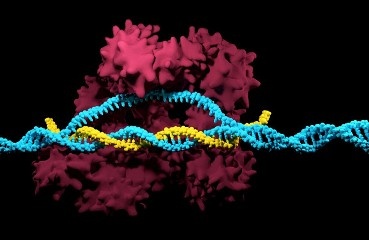 Технологии CRISPR обычно отключают гены, разрушая ДНК в начале целевого гена, вызывая мутации, когда ДНК связывается вместе. Такой подход может вызвать проблемы, такие как разрушение ДНК в местах, отличных от предполагаемой цели, и сломанной ДНК, повторно присоединяющейся к различным хромосомам.
Технологии CRISPR обычно отключают гены, разрушая ДНК в начале целевого гена, вызывая мутации, когда ДНК связывается вместе. Такой подход может вызвать проблемы, такие как разрушение ДНК в местах, отличных от предполагаемой цели, и сломанной ДНК, повторно присоединяющейся к различным хромосомам.
Новый метод CRISPR-SKIP, описанный в журнале Genome Biology, не разрушает нити ДНК, но вместо этого изменяет одну точку в целевой последовательности ДНК.
«Учитывая проблемы с традиционным редактированием генов путем разрушения ДНК, мы должны найти способы оптимизации инструментов для осуществления модификации генов. Это хорошо, потому что мы можем регулировать ген без разрушения геномной ДНК», - сказал профессор биоинженерии штата Иллинойс Пабло Перес- Pinera, который возглавлял исследование с профессором физики Иллинойса Jun Song.
В клетках млекопитающих гены разбиваются на сегменты, называемые экзонами, которые чередуются с областями ДНК, которые, по-видимому, не кодируют ничего. Когда механизм клетки транскрибирует ген в РНК, который должен быть переведен в белок, в последовательности ДНК есть сигналы, указывающие, какие части являются экзонами и которые не являются частью гена. Клетка объединяет РНК, транскрибированную из кодирующих частей, чтобы получить один непрерывный шаблон РНК, который используется для получения белков.
CRISPR-SKIP изменяет одну базу до начала экзона, заставляя клетку читать ее как некодирующую часть.
«Когда клетка лечит экзон в качестве некодирующей ДНК, этот экзон не включается в зрелую РНК, эффективно удаляя соответствующие аминокислоты из белка», - сказал Майкл Гапинске, аспирант биоинженерии и первый автор статьи.
В то время как пропуски экзонов приводят к белкам, которые не хватает нескольких аминокислот, результирующие усеченные белки часто сохраняют частичную или полную активность - этого может быть достаточно, чтобы восстановить функцию при некоторых генетических заболеваниях, сказал Перез-Пинера, который также является профессором в Медицинский колледж Карла Иллинойса. Существуют другие подходы к пропуску экзонов или устранению аминокислот, но поскольку они не навсегда изменяют ДНК, они обеспечивают лишь временную выгоду и требуют повторных введений в течение всего срока жизни пациента, говорят исследователи.
«Редактируя одну базу в геномной ДНК, используя CRISPR-SKIP, мы можем окончательно исключить экзоны и, следовательно, добиться долговременной коррекции заболевания с помощью одного лечения», - сказал Алан Луу, физик-аспирант и один из первых автор исследования. «Этот процесс также обратим, если нам нужно снова включить экзон».
Исследователи протестировали методику в нескольких клеточных линиях от мышей и людей, как здоровых, так и злокачественных.
«Мы протестировали его в трех разных клеточных линиях млекопитающих, чтобы продемонстрировать, что его можно применять к различным типам клеток. Мы также продемонстрировали его в линиях раковых клеток, потому что мы хотели показать, что мы можем нацеливать онкогены», - сказала Сонг.
Они секвенировали ДНК и РНК из обработанных клеток и обнаружили, что система CRISPR-SKIP может ориентироваться на конкретные базы и пропускать экзоны с высокой эффективностью, а также продемонстрировать, что различные целевые CRISPR-SKIP могут быть объединены, чтобы пропускать несколько экзонов в одном гене, если это необходимо. Исследователи надеются проверить свою эффективность на живых животных - первый шаг к оценке его терапевтического потенциала.
«Например, при мышечной дистрофии Дюшенна исправление от 5 до 10 процентов клеток достаточно для достижения терапевтической пользы. С CRISPR-SKIP мы наблюдали изменения скорости более 20-30 процентов во многих клеточных линиях, которые мы изучили», - сказал Перес-Пинера.
Группа построила веб-инструмент, позволяющий другим исследователям искать, может ли экзон быть нацелен на метод CRISPR-SKIP, одновременно минимизируя вероятность его привязки к аналогичным местам в геноме.
Поскольку исследователи увидели некоторые мутации на нецелевых сайтах, они работают над тем, чтобы сделать CRISPR-SKIP еще более эффективным и конкретным.
«Биология сложная: человеческий геном имеет более трех миллиардов баз. Таким образом, вероятность посадки в месте, близком к намеченному региону, не является незначительным и что-то нужно знать с помощью любой технологии редактирования генов», - сказала Сонг. «Причина, по которой мы потратили столько времени, чтобы интенсивно искать ненужные мутации, заключается в том, что это может стать серьезным препятствием для медицинских приложений. Мы надеемся, что будущие усовершенствования технологий редактирования генов увеличат специфичность CRISPR-SKIP, чтобы мы могли начать для решения некоторых проблем, которые не позволили генной терапии широко применяться в клинике».
Источник: https://www.sciencedaily.com/releases/2018/08/180816153147.htm



Комментарии
Пока комментариев нет
Новый комментарий